Perkembangan ekspor udang di
Indonesia telah maju dan pesat khususnya di provinsi Sulawesi Selatan. Pada
tahun 2014 provinsi Sulawesi Selatan mengekspor udang 42.000 ton dalam keadaan
beku ke Amerika, Jepang dan Mesir. Setahun sebelumnya provinsi Sulawesi Selatan
mengekspor udang sebanyak 1.580.981,10 kilogram kesejumlah Negara di dunia (www.sulselprov.go.id).
Data dari dinas perikanan Sulawesi Selatan menyatakan bahwa perkembangan
budidaya udang mulai tahun 2013 semakin pesat karena semakin banyaknya
permintaan ekspor dari Negara-negara lain di dunia.
Peningkatan budidaya perikanan
tahun 2013 sangat bervariasi bergantung pada jenis udang tersebut. Budidaya
udang windu naik 3%, udang vannamei naik 93% serta jenis udang lainnya naik
hingga 22% (www.dpksulsel.net).
Udang yang diekspor berupa udang beku
tanpa kepala dan kulit. Hasil proses pembekuan, 40-50 % dari berat udang
menjadi limbah (kulit dan kepala) yang saat ini masyarakat hanya menggunakannya
sebagai bahan perasa pada pembuatan kerupuk dan terasi (Natsir et al, 2007).
Semakin tingginya presentase budidaya
dan eksporting udang di Sulawesi Selatan dalam bentuk beku menyebabkan semakin
banyaknya limbah udang yang di hasilkan seperti kulit dan kepala udang.
Limbah-limbah tersebut masih kurang termanfaatkan. Oleh karena itu, limbah
tersebut perlu penanganan yang serius terutama karena limbah ini mengandung
senyawa kimia yang berpotensi menjadi bahan yang lebih bermanfaat yaitu kitin
dan kitosan.
Brown dalam Darnianti (2008),
mengemukakan bahawa pengolahan limbah berwawasan lingkungan harus mengikuti
prinsip empat-R yaitu reduce (minimisasi), reuse (pemakaian kembali), recycle
(daur ulang) dan recovery (perolehan kembali). Prinsip daur ulang adalah
pemanfaatan limbah suatu industri menjadi bahan baku oleh industri lain dan
menghasilkan suatu produk baru, contohnya limbah kulit udang dari industri
pemprosesan udang yang dapat diolah menjadi kitin dan kitosan yang merupakan
bahan baku untuk beberapa industri lain.
Sifat kitin yang tidak beracun dan
mudah terdegradasi mendorong dilakukannya modifikasi kitin dengan tujuan
mengoptimalkan kegunaan maupun memperluas bidang aplikasi kitin. Salah satu
senyawa turunan dari kitin yang banyak dikembangkan karena aplikasinya yang
luas adalah kitosan. Kitosan merupakan suatu amina polisakarida dari hasil
deasetilasi kitin. Sifat biokompatibel, biodegradable dan nontoksik yang
dimiliki kitosan, merekomendasikan penggunaan senyawa ini dalam industri ramah
lingkungan.
Kitin dan kitosan yang memiliki
standar mutu tinggi memilki banyak manfaat baik dalan kehidupan rumah tangga maupun
dalam bidang industri. Beberapa manfaat kitosan adalah sebagai agen pengawet
pada makanan, anti bakteri serta sebagai agen pengadsorpsi baik limbah (logam
dan pewarna) maupun zat-zat lain yang memiliki karakter yang sesuai dengan
adsorben kitosan.
Beberapa tahap dalam memperoleh
kitosan yakni : tahap deproteinasi, depmineralisasi, depigmentasi serta tahap
deasetilasi kitin menjadi kitosan. Untuk memperoleh standar mutu kitosan yang
baik perlu diketahui keadaan-keadan optimal pada setiap tahapnya.
Melihat pentingnya mendapatkan
kualitas kitosan yang sesuai dengan standar mutu kitosan, maka penelitian ini
penting dilakukan untuk mengetahui kondisi-konsi optimum pembuatan kitosan pada
setiap tahapannya.
A. Jenis Penelitian
Penelitian ini merupakan penelitian
eksperimen yang bertujuan menentukan kondisi optimum
setiap tahap dalam pembuatan kitosan dari limbah kulit udang putih (Litopenaeus vannamei Bonne).
B.
Waktu dan
Tempat
Penelitian ini mulai dilaksanakan bulan September
2014 yang meliputi penelusuran literatur, observasi mengenai kulit udang, dan
penyusunan proposal. Preparasi dan analisis sampel dilakukan di Laboratorium
Kimia FMIPA UNM.
C.
Objek
Penelitian
Objek dalam penelitian ini adalah
kulit udang putih (Litopenaeus vannamei Bonne).
D. Alat
dan Bahan
1. Alat Penelitian
Alat-alat
yang digunakan pada penelitian ini adalah alat-alat gelas yang umum digunakan, shaker inkubtor
merek Stuart Tipe Orbital Incubator SI500, blender, FTIR, stopwatch, neraca merek Cheetah, oven, dan ayakan (80mesh), cawan, kondensor refluks, kondensor
destilasi, pompa vakum, tanur, dan
eksikator.
2.
Bahan Penelitian
Bahan-bahan yang akan
digunakan pada penelitian ini adalah kulit udang putih, larutan NaOH(p.a), HCl(p.a),
NaOCl(p.a), Indikator universal, H2SO4 (p.a),
Asam Borat(p.a), Indikator PP, KBr(p.a), Pewarna Azo
Direct Biru, aluminium foil, akuades, kertas saring
Whatman, dan Air.
E.
ProsedurPenelitian
1. Penyiapan Sampel
Persiapan dimulai dengan mencuci limbah kulit udang putih yang mentah dengan air berulang kali. Kulit udang dijemur di bawah sinar
matahari sampai benar-benar kering. Kulit udang yang sudah kering kemudian
dihaluskan dengan blender dan di ayak dengan ayakan 80 mesh. Serbuk kulit udang yang lolos ayakan 80 mesh dikeringkan dalam oven pada suhu 105oC selama 1 jam.
2. Penentuan
Kondisi Optimum Setiap Tahap Isolasi Kitin
a.
Deproteinasi
1). Penentuan Perbandingan Optimum NaOH dan
Serbuk Udang
Penentuan ini dilakukan untuk mengetahui perbandingan
optimum yang akan digunakan antara NaOH dan serbuk kulit udang. Variasi
perbandingan (b/v) yang akan gunakan yaitu (1 : 2,5), (1 : 5), (1 : 10), (1 :
12,5) dan (1 : 15). Konsentrasi NaOH pada masing-masing perbandingan adlah 3,5%
yang direaksikan pada suhu 80oC selama 90 menit. Hasilnya dicuci dengan air sampai netral. Setelah netral, larutan disaring. Endapan
dikeringkan dalam oven pada suhu 80oC sampai kering (kurang lebih 24 jam).
2). Penentuan Suhu Optimum
Penentuan suhu
optimum
dilakukan dengan mereaksikan serbuk udang 80 mesh dengan NaOH 3,5% dengan perbandingan optimum yang telah diperoleh. Kemudian larutan di reaksikan pada suhu yang bervariasi antara 70, 80, 90, 100, dan 120oC selama 90 menit. Hasilnya dicuci dengan air sampai
netral. Setelah netral, larutan disaring. Endapan dikeringkan dalam oven pada
suhu 80oC sampai kering (kurang lebih 24 jam).
3). Penentuan Waktu Optimum
Penentuan waktu
optimum
dilakukan dengan mereaksikan serbuk udang 80 mesh dengan NaOH 3,5% dengan perbandingan optimum yang telah diperoleh. Kemudian larutan di reaksikan pada suhu optimum (dari prosedur sebelumnya) selama 60, 90, 120, 240, dan 360 menit. Hasilnya dicuci dengan air sampai netral. Setelah netral, larutan disaring. Endapan
dikeringkan dalam oven pada suhu 80oC sampai kering (kurang lebih 24 jam).
4). Penentuan Konsentrasi Optimum
Penentuan
konsentrasi optimum dilakukan dengan mereaksikan serbuk udang 80 mesh dengan NaOH 2,5
; 3,5 ; 5 ; 7 dan 8% dengan perbandingan optimum
yang telah diperoleh. Kemudian larutan di reaksikan pada suhu optimum (dari prosedur sebelumnya) selama rentang waktu optimum. Hasilnya dicuci dengan air sampai
netral. Setelah netral, larutan disaring. Endapan dikeringkan dalam oven pada suhu
80oC sampai kering (kurang lebih 24 jam).
b.
Demineralisasi
1). Penentuan Perbandingan Optimum HCl dan
Serbuk Udang
Penentuan ini dilakukan untuk mengetahui perbandingan
optimum yang akan digunakan antara HCl dan serbuk kulit udang hasil
deproteinasi. Variasi perbandingan (b/v) yang akan gunakan yaitu (1 : 2,5), (1
: 5), (1 : 10), (1 : 12,5) dan (1 : 15). Konsentrasi HCl pada masing-masing
perbandingan adalah 1M yang direaksikan pada suhu 80oC selama 90
menit. Hasilnya dicuci dengan air sampai netral. Setelah netral, larutan
disaring. Endapan dikeringkan dalam oven pada suhu 80oC sampai kering (kurang lebih 24 jam).
2). Penentuan Suhu Optimum
Penentuan suhu optimum dilakukan dengan mereaksikan serbuk hasil deproteinasi dengan HCl 1M dengan perbandingan optimum yang telah diperoleh. Kemudian larutan di reaksikan pada suhu yang bervariasi antara 70, 80, 90, 100, dan 120oC selama 90 menit. Hasilnya dicuci dengan air sampai
netral. Setelah netral, larutan disaring. Endapan dikeringkan dalam oven pada
suhu 80oC sampai kering (kurang lebih 24 jam).
3). Penentuan Waktu Optimum
Penentuan waktu optimum dilakukan dengan mereaksikan serbuk hasil deproteinasi dengan HCl 1M dengan perbandingan optimum yang telah diperoleh. Kemudian larutan di reaksikan pada suhu optimum (dari prosedur sebelumnya) selama 60, 90, 120, 240, dan 360 menit. Hasilnya dicuci dengan air sampai netral. Setelah netral, larutan disaring. Endapan
dikeringkan dalam oven pada suhu 80oC sampai kering (kurang lebih 24 jam).
4). Penentuan Konsentrasi Optimum
Penentuan konsentrasi optimum dilakukan dengan mereaksikan
serbuk hasil deproteinasi
dengan HCl 0,25; 0,50; 1,00; 1,25;
dan 1,50 M
dengan perbandingan optimum yang
telah diperoleh.
Kemudian larutan di reaksikan pada suhu optimum (dari prosedur sebelumnya) selama rentang waktu optimum. Hasilnya dicuci dengan air sampai
netral. Setelah netral, larutan disaring. Endapan dikeringkan dalam oven pada
suhu 80oC sampai kering (kurang lebih 24 jam).
c.
Deasetilasi
1). Penentuan Perbandingan Optimum NaOH dan
Kitin
Penentuan ini dilakukan untuk mengetahui perbandingan
optimum yang akan digunakan antara NaOH dan kitin. Variasi perbandingan (b/v)
yang akan gunakan yaitu (1 : 2,5), (1 : 5), (1 : 10), (1 : 12,5) dan (1 : 15).
Konsentrasi NaOH pada masing-masing perbandingan adalah 50% yang direaksikan
pada suhu 80oC selama 90 menit. Hasilnya dicuci dengan air sampai
netral. Setelah netral, larutan disaring. Endapan dikeringkan dalam oven pada
suhu 80oC sampai kering (kurang lebih 24 jam).
2). Penentuan Suhu Optimum
Penentuan suhu optimum dilakukan dengan mereaksikan kitin dengan NaOH
50% dengan
perbandingan optimum yang
telah diperoleh.
Kemudian larutan di reaksikan pada suhu yang bervariasi antara 70, 80, 90, 100, dan 120oC selama 90 menit. Hasilnya dicuci dengan air sampai
netral. Setelah netral, larutan disaring. Endapan dikeringkan dalam oven pada
suhu 80oC sampai kering (kurang lebih 24 jam).
3). Penentuan Waktu Optimum
Penentuan waktu optimum dilakukan dengan mereaksikan kitin dengan NaOH
50% dengan
perbandingan optimum yang
telah diperoleh.
Kemudian larutan di reaksikan pada suhu optimum (dari prosedur sebelumnya) selama 60, 90, 120, 240, dan 360 menit. Hasilnya dicuci dengan air sampai netral. Setelah netral, larutan disaring. Endapan
dikeringkan dalam oven pada suhu 80oC sampai kering (kurang lebih 24 jam).
4). Penentuan Konsentrasi Optimum
Penentuan konsentrasi optimum dilakukan dengan mereaksikan kitin dengan NaOH 40, 45, 50, 55, dan 60% dengan perbandingan optimum yang telah diperoleh. Kemudian larutan di reaksikan pada suhu optimum (dari prosedur sebelumnya) selama rentang waktu optimum. Hasilnya dicuci dengan air sampai
netral. Setelah netral, larutan disaring. Endapan dikeringkan dalam oven pada
suhu 80oC sampai kering (kurang lebih 24 jam).
3. Penentuan
Karakteristik Kitin dan Kitosan
Penentuan
karakteristik kitin dilakukan untuk mengetahui bahwa senyawa yang diperoleh
dari hasil isolasi limbah udang adalah kitin dan kitosan, yaitu dengan cara
sebagai berikut :
a.
Uji
Kadar Air
Sampel kitin dan
kitosan yang diperoleh dari hasil isolasi kitin ditimbang sebanyak 0,5 gram dan
dimasukkan dalam wadah (Cawan Porselin) yang telah diketahui berat kosongnya
kemudian ditimbang lagi. Setelah itu diovenkan pada suhu 105oC
selama 2 jam, kemudian didinginkan dalam eksikator selama 30 menit lalu
ditimbang lagi. Perlakuan ini dilakukan hingga beratnya konstan yakni selisih penimbangan
0,002 di tiga kali penimbangan terakhir. Kadar air dapat dihitung dengan rumus berikut :
b.
Uji
Kadar Abu
Sampel kitin dan kitosan yang diperoleh dari hasil
isolasi kitin ditimbang sebanyak 0,5 gram dan dimasukkan dalam wadah (Cawan
Porselin) yang telah diketahui berat kosongnya kemudian ditimbang lagi. Sampel
kemudian dipanaskan dalam tanur hingga 500oC selama 30-45 menit.
Dari 500oC dinaikkan menjadi 900oC selama 60-90 menit dan
dipertahankan pada suhu 900oC. Sampel hasil pemanasan lalu
didinginkan di plat logam (10 menit) dan dieksikator (15 menit) lalu ditimbang.
Untuk menghitung kadar abu digunakan rumus sebagai berikut :
c.
Analisis
N-Total
Analisis kadar
protein dilakukan dengan metode kjeldahl.
Sampel ditimbang sebanyak 5 gram kemudian dimasukkan kedalam labu kjeldahl.
Ditambahkan 0,5 gram selenium dan 35 mL H2SO4 (p),
kemudian didestruksi sampai larutan jernih. Larutan didinginkan kemudian
ditambahkan dengan 200 mL air. Larutan tersebut
dimaksukkan kedalam labu destilasi kemudian dimasukkan beberapa tetes indikator
phenofthalein. Ditambahkan NaOH 45% sampai larutan bersifat basa kemudian labu
dihubungkan dengan dengan alat destilasi. Larutan lalu didestilasi sampai destilat
yang diperoleh sebanyak 100 mL. Destilat yang diperoleh ditampung dalam 25 mL
asam borat 3% sampai volume 100 mL. Destilat lalu ditambahkan dengan 3 tetes
indikator campuran. Destilat tersebut lalu dititrasi dengan larutan standar HCl
0,1 N sampai warna ungu (catat volume titrasi). Hal yang sama juga dilakukan
terhadap blangko. Kadar protein dapat dihitung dengan menggunakan rumus :
d.
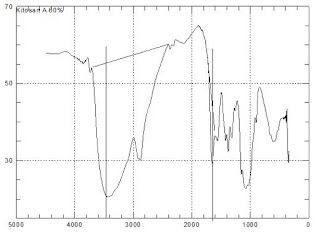
Analisis
dengan Spektroskopi Infra Merah
Spektrum kitin diperoleh dengan menggunakan
spketroskopi IR dengan sampel berupa padatan. Disiapkan serbuk udang hasil
deproteinasi yang kemudian dicampurkan dengan KBr kering. Campuran tersebut di
tumbuk hingga diperoleh ukuran partikel yang kecil. Sampel yang telah
dihaluskan kemudian dimasukkan kedalam pellet
press secara merata. Kemudian pellet press dihubungkan ke pompa hidrolik
dengan kekuatan 100 ton (kg newton) serta dipompa vakum selama 15 menit.
Diusahakan pellet dibuka secara
hati-hati, kemudian pellet yang
dihasilkan dipindahkan dengan menggunakan spatula ke dalam sel holder. Serapan
sampel selanjutnya diukur dengan FTIR. Data serapan yang dihasilkan digunakan
untuk menganalisis gugus fungsi yang muncul serta untuk menghitung derajat
deasetilasi dari kitin. Prosedur yang sama juga dilakukan untuk kitosan.
DAFTAR PUSTAKA
Arif, Abdul Rahman. 2013. Potensi Kitin Deasetilasi Dari (Bacillus Licheniformis) HSA3-1A Untuk
Produksi Kitosan Dari Limbah Udang Putih (Pheaneus merguiensis) Sebagai Bahan
Pengawet Bakso Ikan. Makassar : Pascasarjana Universitas Hasanuddin.
Bastaman. 1990. Penelitian Limbah Udang
sebagai Bahan Industri Khitin dan Khitosan. Kementerian Perindustrian. BBIHP.
Bogor.
Darnianti,
2008, Penurunan Kadar Warna Limbah Cair
Industri Pencucian Jeans Dengan Kitosan dan Jamur Lapuk Putih (Trametes
versicolor). Medan : Pascasarjana Universitas Sumatera Utara.
Departemen Perikanan dan Kelautan Sulawesi Selatan,
2015. Perkembangan Budidaya Udang
Sulawesi Selatan Tahun 2013. url : http://dpksulsel.net/
Focher, B. et.al, 1992.
Structural Differences Between Chitin Polymorphs and Their Precipitates from
Solution Evidence from CP-MAS 13 C-NMR, FT-IR and FT-Raman Spectroscopy. Journal Charbohidrat Polymer. 17 (2) : 97 – 102.
Komardi,
Ahmad, 2007. Potensi Usaha Budidaya Udang
Putih (Litopenaeus Vannamei Bonne) Di Wilayah Pesisir Pantai Timur Kabupaten
Tulang Bawang Lampung Dan Kabupaten Ogan Komering Ilir Sumatera Selatan.
Lampung: Keahlian Perikanan, Universitas Terbuka UPBJJ Lampung.
Lee, JY et al, 2002.
Enhanced Bone Formation by Controlled Growth Factor Delivery From Chitosan –
Based Biomaterials. Journal of Controlled
Release. 17 January 2002, Vol.78 (1): 187-197
Natsir, H, et.al. 2007. Konversi Kitin dari Limbah Udang Api-api
(Metapenaeus monoceros) Menjadi Senyawa Kitosan Secara Enzimatis. Jurnal Marina Chemica
Acta. Edisi Khusus Seminar Nasional FK3TI: 82–89
No HK, Meyers SP., & Lee KS. 1989. Isolation and Characterization
of Chitin from Crawfish Shell Waste. J
Agri Food Chem 37: 575-579
Pemerintah Provinsi Sulawesi Selatan, 2015. Sulsel
Ekspor 42.000 Ton Udang Beku ke Amerika, Jepang dan Mesir Tahun 2014. url: http://sulselprov.go.id/berita/
Prasetyaningrum A et
al, 2007. Optimasi Derajat Deasetilasi Pada Proses Pembuatan Chitosan dan
Pengaruhnya Sebagai Pengawet Pangan. Jurnal
Riptek, Vol,1 No.1, November 2007, Hal: 39-46
Puspitasari, Anggraini, 2007. Pembuatan Dan Pemanfaatan Kitosan Sulfat Dari Cangkang Bekicot
(Achatina Fullica) Sebagai Adsorben Zat Warna Remazol Yellow FG 6.
Surakarta : FMIPA Universitas Sebelas Maret.
Rochima, Emma, 2014. Kajian Pemanfaatan Limbah
Rajungan dan Aplikasinya untuk Bahan Minuman Kesehatan Berbasis Kitosan. Jurnal Akuatika Vol.1 No.1/ Maret 2014
(71-82) ISSN 0853-2532
Sanjaya,I dan Yuanita.L. 2007. Adsorpsi Pb (II) oleh
Kitosan Hasil Isolasi Kitin Cangkang Kepiting Bakau (Scylla sp). Jurnal Ilmu Dasar, Vol.8 No.1 hal. 31.
2007.
Sanusi, Mustari, 2004. Transformasi Kitin Dari Hasil
Isolasi Limbah Industri Udang Beku Menjadi Kitosan. Marina Chimica Acta, Oktober 2004, hal. 28-32. Vol. 5 No.2 ISSN
1411-2132
Savitri Emma et
al, 2010. Sintesis Kitosan, Poli (2-amino-2-deoksi-D-Glukosa), Skala Pilot Project dari Limbah Kulit Udang
sebagai Bahan Baku Alternatif Pembuatan Biopolimer.
Prosiding Seminar Nasional Teknik Kimia
Kejuangan. ISSN 1693-4393
Suhartono, M.T, 2006. Pemanfaatan Kitin, Kitosan, Kitooligosakarida. Jurnal Foodreview 1 (6): 30-33

Komentar
Posting Komentar